M.D.M PUBLIC SCHOOL JANI KHURD
HOME ASSIGNMENT
SESSION – 2020 – 2021
CLASS – 10th
SUBJECT – CHEMISTRY
SUBJECT TEACHER - RAJ KUMAR SIR
SUBJECT TEACHER - RAJ KUMAR SIR
पाठ - 1 कक्षा - 10
रासायनिक अभिक्रियाएँ और समीकरण
रासायनिक अभिक्रियाएँ और समीकरण CHEMICAL REACTION AND EQUATION
भौतिक परिवर्तन (Physical changes) :- वे परिवर्तन जिनमे पदार्थो के भौतिक गुण जैसे - आकर, रंग , अवस्था , ताप आदि अस्थाई रूप से बदल जाते है परन्तु उनके भार और संघटन मे कोई परिवर्तन नहीं आता और न कोई नया पदार्थ बनता , भौतिक परिवर्तन कहलाते है |
जैसे :- पदार्थो का गलना , जमना ,द्रवण, आसवन , मोम का पिंघलना , कपड़ो का सुखना , प्लास्टिक से खिलौने बनाना , पानी गर्म करना |
रासायनिक परिवर्तन (Chemical changes) :- वे परिवर्तन जिनमे [पदार्थ सदैव के लिए बदलकर नए पदार्थो मे बदल जाते है तथा नए पदार्थो का भार , संघटन ,भौतिक व रसायनिक गुण मूल पदार्थो से सदा अलग रहते हो, रसायनिक परिवर्तन कहलाते है |
जैसे :- मोम बत्ती का जलना , कागज का जलना , कार्बन डाई ऑक्साइड का बनना, जंग का लगना ,बिना बुझे चुने से बुझा हुआ चुने का बनना आदि |
ऊपर दिए गए सभी इमेज मे कुछ रासायनिक परिवर्तन है और कुछ भौतिक परिवर्तन हे |
रासायनिक अभिक्रियाएँ (Chemical Reaction) :- पदार्थो मे रासायनिक परिवर्तन के समय होने वाली क्रिया को रासायनिक अभिक्रिया कहते है |
दूसरे शब्दों मे , जब एक या एक से अधिक पदार्थ परस्पर अभिक्रिया करके नए पदार्थ बनाते है जिनके भौतिक व रासायनिक गुण मूल पदार्थो से हमेशा अलग होते है , तो ऐसी अभिक्रिया को रासायनिक अभिक्रिया कहते है |
जैसे :- कार्बन को जलने पर कार्बन डाई ऑक्साइड जाती है |
रासायनिक समीकरण (Chemical Equation) :- रासायनिक अभिक्रिया को प्रतीकों द्वारा प्रदर्शित करने का तरीका रासायनिक समीकरण कहते है |
जैसे :-
अभिकारक (Reactants) :- जो पदार्थ रासायनिक अभिक्रिया करने को लिए जाते है उन्हें अभिकारक कहते है | बायीं तरफ जो प्रतिक लिखे जाते है|
उत्पाद (Product) :- रासायनिक अभिक्रिया के फलस्वरूप जो पदार्थ बनता है , उसे उत्पाद कहते है | उत्पाद दायी तरफ लिखा जाता है |
जैसे :-
यदि अभी भी आपकी कोई समस्या है तो हमारा ये देखे |
रसायनिक रासायनिक समीकरण को संतुलित करना
आइये बताते रासायनिक समीकरण को कैसे संतुलित करे |
आइये बताते रासायनिक समीकरण को कैसे संतुलित करे |
- सबसे पहले आप सभी यौगिकों के चारो और एक बॉक्स बना ले |
- विभिन्न परमाणुओं संख्या एक सूचि मे लिख ले |
- सुविधा के सबसे पहले आप उस परमाणु को संतुलित करे जो ज्यादा हो , वह अभिकारक हो या उत्पाद की तरफ |
- अब आप सभी परमाणुओ को एक बार चेक कर ले वो सभी दोनों साइड मे बराबर है या नहीं |
- बराबर नहीं है तो आप उचित संख्या से गुणा करके बराबर कर दे |
रासायनिक समीकरणों के प्रकार
(1) संयोजन या योगात्मक अभिक्रियाएँ (Addition Reactions) :- वे रासायनिक अभिक्रियाएँ जिनमे दो या दो से अधिक पदार्थ आपस मे संयोग करके केवल एक नया पदार्थ बनाते है , योगात्मक या संयोजन अभिक्रिया कहलाती है |
2Mg(s) + O2(g) ⟶ 2MgO(s)
(2) अपघटन अभिक्रियाएँ (Decomposition Reactions) :- वे अभिक्रियाएँ जिनमे एक बड़ा यौगिक किसी बाह्य करक की उपस्तिथि मे दो या दो से अधिक छोटे यौगिकों मे टूट जाता है |
(a)उष्मीय अपघटन (Thermal Decomposition) :- ताप के प्रभाव से जो अपघटन होता है उसे उष्मीय अपघटन कहते है |
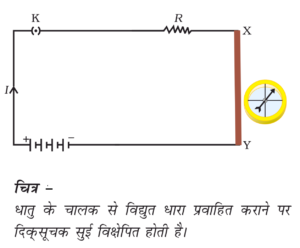
(b)विद्युतीय अपघटन (Electrolysis Decomposition) : - जब पदार्थ के जलीय विलयन मे विद्युत धारा से अपघटन किया जाता है उसे विधुतीय अपघटन कहते है |
(c)प्रकाशीय अपघटन(Photo Decomposing Reaction) :- जो अपघटन प्रकाश की उपस्थिति मे होता है उसे प्रकाशीय अपघटन कहते है |
(3) विस्थापन अभिक्रियाएँ (Displacement Reaction) :- वे रासायनिक अभिक्रियाएँ जिनमे किसी यौगिक में उपस्थित परमाणु या अणु कम क्रियाशील परमाणु या अणु को विस्थापित कर देता है |
(4) द्विविस्थापन अभिक्रिया (Double Displacement) :- ऐसी अभिक्रियाएँ जन्मे दो यौगिक इस प्रकार क्रिया करते है कि उनके आयनो या घटको की अदला - बदली जाती है तथा नए यौगिक बनते है ,द्विविस्थापन अभिक्रिया कहलाती है |
(5) वियोजन अभिक्रियाएँ (Dissociation Reaction) :- वह अभिक्रियाएँ जिनमे कोई पदार्थ रसायनिक अभिक्रिया को प्रेरित करने वाले कारणों ( जैसे - ताप दाब आदि ) आदि में परिवर्तन करने से दो या अधिक पदार्थो में अपघटित हो जाता हो तथा कारन हटा लेने के बाद वह पुन : मूल पदार्थ बन जाता हो , वियोजन अभिक्रिया कहलाती है |
वियोजन निम्न प्रकार से सकता है ---उष्मीय वियोजन (Thermal Dissociation) :- जब यौगिकों को गर्म करने से उनका अपघटन हो जाता है तो इस प्रकार के अपघटन को उष्मीय अपघटन कहते है |
आयनिक अपघटन (Ionic Dissociation) :- जब विद्युत संयोजक पदार्थो को जल मे घोला जाता है तो वह अपने आयनो मे टूट जाता है उसमे एक धनायन और एक ऋणायन बनता है , ये आयन पुन : संयोग करके उदासीन लवण बना लेते है | इस वियोजन को आयनिक वियोजन या विद्युत अपघटनी वियोजन कहते है |
(6)ऊष्माक्षेपी तथा ऊष्माशोषी अभिक्रियाएँ ऊर्जा परिवर्तन के आधार पर अभिक्रियाओं को दो भागो मे बांटा गया है -
(a) ऊष्माक्षेपी अभिक्रिया (Exothermic Reaction) :- वे अभिक्रियाएँ जिनमे ऊष्मा का उत्सर्जन होता है , ऊष्माक्षेपी अभिक्रियाएँ कहलाती है इनमें ऊष्मा की मात्रा को उत्पादों की ओर धन चिन्ह (+) के साथ दर्शाया जाता है | जैसे
(b) ऊष्माशोषी अभिक्रिया (Endothermic Reaction) :- वे अभिक्रियाएँ जिनमे ऊष्मा का अवशोषण होता है , ऊष्माशोषी अभिक्रिया कहलाती है | ऊष्माशोषी अभिक्रिया निम्न ताप पर अस्वत: होती है तथा उच्च ताप पर स्वत: होती है | इनमें ऊष्मा की मात्रा को उत्पादों की ओर ऋण चिन्ह (-) के साथ दर्शाया जाता है |
(7) उदासीनीकरण अभिक्रियाएँ (Neutralization Reaction) :- वे रासायनिक अभिक्रियाएँ जिनमे उचित अम्ल और उचित क्षार आपस मे क्रिया करके एक दूसरे के प्रभाव को नस्ट कर देते है , उदासीनीकरण अभिक्रिया कहलाती है |
ऑक्सीकरण (उपचयन) :- वह अभिक्रिया जिसमे कोई पदार्थ ऑक्सीजन से क्रिया करता है या हाइड्रोजन को अलग करता है | इस प्रक्रिया को ऑक्सीकरण या उपचयन कहते है |
अपचयन :- वह अभिक्रिया जिसमे कोई पदार्थ हाइड्रोजन से क्रिया करता हो या फिर ऑक्सीजन को अलग करता हो इस प्रक्रिया को अपचयन कहते है |
संक्षारण (Corrosion)
वह प्रक्रिया जिसमे कोई पदार्थ नमी ,वायु आदि से क्रिया करके अपनी चमक खो दे और उस पदार्थ का क्षय हो जाये , संक्षारण कहलाती है |
जैसे :- लोहे पर जंग का लगना ,चाँदी का काला पड जाना
विकृतिगंधिता (Rancidity)
जब खाद्य पदार्थो में उपस्तिथ तैल या वसा की वायु की उपस्तिथि में अपचयन हो जाने से उसमे दुर्गन्ध उत्पन्न हो जाती है , यह प्रक्रिया विकृतिगंधिता कहलाती है |
किसी भी तरह की शिकायत या हैल्प के लिए संपर्क करे | - 8126271896 ( 3:00 PM TO 5:00 PM )
LESSION COMPLETE
- Chapter 2 - CLICK HERE
- Chapter 3 - CLICK HERE
CHEMISTRY FOR CLASS 9th
पाठ-१ हमारे आस पास के पदार्थ | पदार्थ (द्रव्य) क्या है ? CLASS 9TH - CLICK HERE
पाठ - 2 क्या हमारे आस - पास के पदार्थ शुद्ध है CLASS 9TH CH 2 - CLICK HERE
पाठ - 3 परमाणु और अणु - CLICK HERE
PHYSICS FOR CLASS 9th
पाठ - 8 गति CLASS 9TH - CLICK HERE
पाठ - 9 बल तथा गति के नियम - CLICK HERE
पाठ - 10 गुरुत्वाकर्षण (GRAVITY 9TH CLASS ) - CLICK HERE
पाठ - 11 कार्य तथा ऊर्जा (work and energy) - CLICK HERE
CHEMISTRY FOR CLASS 10th
पाठ - 1 रासायनिक अभिक्रियाएँ और समीकरण - CLICK HERE
पाठ-2 अम्ल व क्षार ( ACID AND BASE ) - CLICK HERE
पाठ - 3 धातु और अधातु - CLICK HERE
पाठ - 4 कार्बन व उसके यौगिक - CLICK HERE
किसी भी तरह की शिकायत या हैल्प के लिए संपर्क करे | - 8126271896 ( 3:00 PM TO 5:00 PM )
पाठ - 1 रासायनिक अभिक्रियाएँ और समीकरण - CLICK HERE
पाठ-2 अम्ल व क्षार ( ACID AND BASE ) - CLICK HERE
पाठ - 3 धातु और अधातु (Mattel And Non Mattel) - CLICK HERE
पाठ - 4 कार्बन व उसके यौगिक - CLICK HERE



















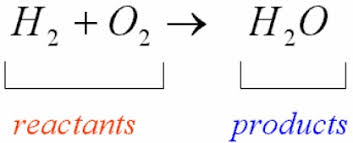
















No comments:
Post a Comment